Así se descubrió la muerte de 16 niños en la Clínica Laura Daniela
Un funcionario de la misma clínica alertó sobre las anomalías al fabricante del medicamento utilizado para la estabilización respiratoria de bebés prematuros. Una delegada de Abbvie Laboratories llegó a Valledupar y presentó la denuncia ante la Secretaría de Salud Departamental, que solo tres meses después abrió la investigación.
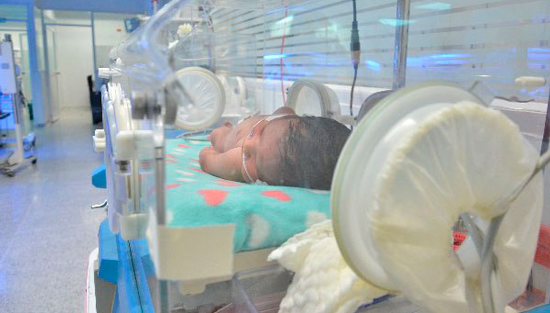
Quizá, si el gerente del Hospital Rosario Pumarejo de López, Armando Almeira Quiroz, hubiese tenido con mayor anterioridad la oportunidad de dar a conocer al Invima (Instituto Nacional de Vigilancia de Medicamentos y Alimentos) y a la Secretaría Salud Departamental irregularidades en el medicamento Survanta, utilizado en la Clínica Laura Daniela de Valledupar, las vidas de 16 recién nacidos, que hoy están muertos, podían haber tenido un futuro distinto.
Una pediatra del Rosario Pumarejo encontró en el surfactante (medicamento) pulmonar características físicas adulteradas, entre ellas la viscosidad y el color. Es de decir, el empaque estaba adulterado y por ende, la fórmula química no tendría el efecto esperado en los pacientes.
Almeira Quiroz no fue el único que se percató de la anomalía ese 25 de noviembre de 2016. Diez días antes, el 15 de noviembre, Nubia Dalila Pachón Orozco, funcionaria de Juritech & Co Ltda, empresa asesora externa en la seguridad del Departamento de Global Protection Products GPP de Abbvie Laboratories inc., con sede en Chicago, Estados Unidos, presentó una queja o denuncia ante la Secretaría de Salud Departamental en relación con la compra y posterior distribución o dispensación del producto denominado Synagis Palivizymab 50 mg, de propiedad de Abbvie Laboratories, fármaco que ayuda a la maduración de los pulmones de neonatos y niños con pocos meses de vida, al igual que para evitar una enfermedad grave del aparato respiratorio inferior (pulmón).
En la denuncia hecha por Pachón Orozco se asegura que a pesar de no ser el mismo Survanta aplicado a los 16 niños muertos, fue un regente de la Clínica Laura Daniela de Valledupar, que el 3 de octubre de 2016, se comunicó con Abbvie Laboratories y puso en conocimiento que el Synagis identificado con Lote N° 381255X, no se encontraba en buenas condiciones y “tenía apariencia de que ya lo hubiesen utilizado”.
https://noticias.caracoltv.com/septimo-dia
El funcionario envió a Abbvie Laboratories un material fotográfico, luego la entidad internacional dictaminó que “este es falsificado”. Finalmente, a la persona que hizo llegar las pruebas a Estados Unidos, la Clínica Laura Daniela lo habría retirado del cargo. Después la Secretaría de Salud Departamental intervino en el asunto, en una visita de inspección donde no encontró mayores anomalías.
Teniendo como base las denuncias de Nubia Pachón Orozco y la de Armando Almeira, solo hasta el 3 de febrero del 2017 la Secretaría de Salud Departamental, por medio de la Oficina de Vigilancia y Control de Medicamento, abrió investigación formal a la Clínica Integral de Emergencia Laura Daniela, representada legalmente por Jaime Arce García.
Para esa época, ya el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) en conjunto a la Fiscalía General de la Nación, había adelantado una diligencia de inspección, vigilancia y control a la entidad prestadora de salud, ubicada en la carrera 19 con calle 14 de la capital del Cesar.
16 muertes en seis meses
El 26 de enero de 2017, el Invima y algunos funcionarios de la Fiscalía llegaron a la Secretaría de Salud Departamental, pidieron acompañamiento y posteriormente se trasladaron a la Clínica Laura Daniela.
De manera exclusiva, EL PILÓN tuvo acceso a las conclusiones recogidas una vez terminó la visita de seguimiento a la Clínica Integral de Emergencias Laura Daniela, como seguimiento a la resolución concedida por el Invima de Buenas Prácticas de Elaboración.
El Invima hizo un recorrido general por las instalaciones de la Laura Daniela, de esa manera los profesionales de la Dirección de Medicamentos y Productos Biológicos de la entidad conceptuaron que la Clínica Laura Daniela “no mantiene las condiciones bajo las cuales se otorgó la certificación respectiva (…), no cumple con las Buenas Prácticas de Elaboración para los procesos y actividades certificadas en dicha resolución”.
El acta final fue firmada por Sahin Oswaldo Ochoa y Agustín Sánchez Mora por Invima, mientras que Álex Bolaño Lara, Sergio Polo y María Paulina Martínez, lo hicieron por la Clínica Laura Daniela.
Esa misma pesquisa sirvió como visita de inspección sanitaria en atención a solicitud de la Dirección de Medicamentos y Productos Biológicos, relacionada con la comercialización del medicamento Survanta amparado con registro sanitario 2013M-014168-R1 de procedencia presuntamente fraudulenta.
La denuncia ante el Invima fue de Abbvie, los mismos que por medio de un delegado la entregaron a la Secretaría de Salud Departamental, el 15 de noviembre de 2016. El proceso de investigación fue radicado además en la Fiscalía General de la Nación en el marco del proceso de falsificación del medicamento Survanta 8 ml. El allanamiento fue hecho por las autoridades competentes el 27 de enero de 2017, encontrando los productos antes mencionados, los cuales fueron objeto de decomiso.
El Invima argumentó que la Clínica Laura Daniela contaba con servicio UCI neonatal en grado de complejidad media, relacionada con el uso del medicamento Survanta establecido en el registro sanitario y en los lotes que fueron identificados por el laboratorio fabricante como fraudulento.
“El representante de la laboratorios Abbvie realizó la comparación del producto que se tenía en inventario, el cual fue comparado contra el medicamento de la casa matriz, el personal de la casa matriz (perito) realizó la verificación con un equipo especializado, manifestando que el producto que se encontraba en las instalaciones (Clínica Laura Daniela) no era el original. Lo anterior, de acuerdo a lo manifestado en la comparación del mapa biométrico y otras características de las tintas no corresponden con el producto original, a su vez se observa segmentación en las tinta y errores ortográficos, entre otros”, indica el informe del Invima, entregado el 26 de enero del presente año.
“En total fueron 37 unidades para el lote 1043809”, agrega el documento que cuando los funcionarios indagaron frente a la aplicación del producto y estado actual de los pacientes, obtuvieron los siguientes resultados:
* “El producto fue adquirido desde junio de 2016 hasta la fecha de la visita (26 de enero de 2017).
* La misma cantidad de neonatos recibieron el medicamento Survanta con lote 10433809: 24.
* Total de niños a los que se les administró el medicamento Survanta con lote 10433809 y que se encuentran vivos a la fecha: 8.
* Total de niños a los que se les administró el medicamento Survanta con lote 10433809 fallecidos a la fecha: 16”.
La muerte de los niños comenzó el 28 de junio de 2016, ese día se presentó el deceso de un infante de 30 semanas de nacido, así mismo fallecieron 15 más en edades promedio de 38, 40.2, 36 y 29.4 semanas. El último que pereció, a la fecha de dicho perito, fue el 24 de enero de 2017, después de permanecer seis días en la UCI neonatal de la Clínica Laura Daniela y haber recibido el medicamento antes mencionado.
La Clínica Laura Daniela le dijo al Invima que los proveedores de los productos eran Farmapos y VC Medical; el primero suministró dos unidades y el segundo, 35. Finalmente el CTI de la Fiscalía decomisó 11 unidades del producto.
Después de llegar a la Clínica Laura Daniela, el Invima aplicó medida sanitaria a Osmany Ricardo Córdoba Peña, propietario del establecimiento de comercio VC Medical.
El hecho se dio el 9 de febrero de 2017, en la diagonal 16B bis # 23B-79 de Valledupar. Allí el Invima por solicitud extraordinaria realizada por el Cuerpo Técnico de Investigación CTI de la Fiscalía General de la Nación, allanó las instalaciones del lugar en una inspección sanitaria.
El CTI encontró varias anomalías, como que el sitio no cumplía con las condiciones higiénicas, técnicas, locativas, de dotación, recursos humanos y verificación de calidad control de calidad, que garantizaran el adecuado manejo de los dispositivos médicos.
Comienzo de la tragedia
“El 25 de noviembre un niño prematuro, de bajo peso al nacer, necesitaba que se le suministrara Survanta, la neonatóloga que lo aplica se percata que las características físicas y químicas del medicamento son diferentes a las acostumbradas. En ese momento, teniendo en cuenta las diferencias, nos dirigimos y llenamos el formato que se debe diligenciar, prácticamente es una denuncia ante el Invima y poner en conocimiento a la Secretaría de Salud y al mismo laboratorio”, declaró el gerente del Hospital Rosario Pumarejo de López, Armando Almeira Quiroz.
El funcionario explicó en diálogo con EL PILÓN que en las instalaciones nada más tenían dos frascos de Survanta, por los bajos recursos que la entidad tenía para comprar un medicamento de alto costo.
“La Fiscalía vino y realizó un recorrido por la farmacia, no encontró más nada, y se llevó el otro frasco para hacerse el respectivo procedimiento. El medicamento fue adquirido directamente por el hospital a través de una distribuidora que se llama Farmapos (Distribuidora Farmapos S.A.S)”, resaltó Almeira Quiroz, quien dijo no tener información si el lote de su Survanta era igual a los aplicados y además decomisados por el CTI, en la Clínica Laura Daniela.
“Lo primero que hice fue retirar el medicamento, lo segundo fue no comprarle más medicamento a quien lo suministró, después poner las quejas o denuncias ante las entidades respectivas y luego de eso consideramos que el Invima, encargado de hacer el proceso a nivel nacional, es quien debe hacer un informe que al hospital no ha llegado de manera oficial”, recalcó.
La clínica
La Clínica Laura Daniela emitió un comunicado donde se pronuncia sobre las denuncias hechas por el programa Séptimo Día, emitido la noche del domingo por Caracol Televisión.
Rechazaron las afirmaciones de dicho informe y sostienen “que se busca responsabilizar a la institución de hechos que se encuentran en proceso de investigación”.
“La clínica es en primer lugar la más interesada en continuar con el proceso de investigación llevado por las autoridades competentes para que se confirme que no existe ninguna correlación entre el medicamento y la muerte de 16 menores de edad durante el periodo transcurrido entre junio de 2016 y enero de 2017; para ello, hemos tenido la mayor disposición ante los organismos de control tales como Secretaría de Salud Departamental, Secretaría de Salud Municipal, Invima, Superintendencia Nacional de Salud y Fiscalía, quienes han hecho trazabilidad de toda la información solicitada para el caso”.
Se destacan como “una institución reconocida por su seriedad y responsabilidad”, basándose en “que se pagó el valor estandarizado en el mercado (del producto), por ende se demuestra que fue violentada nuestra buena fe por un proveedor de medicamentos al cual denunciamos ante las autoridades de manera oportuna y contundente”.
Reiteraron su misión de “salvar vidas, haciendo mérito al servicio humanizado por vocación e integralidad”, así como también señalaron que “en la unidad materno-infantil somos centro de referencia de la región, con un promedio de nacidos vivos de aproximadamente 300 neonatos por mes”.
Así va el proceso
EL PILÓN conoció que el 16 de agosto de 2017, la Secretaría de Salud Departamental formuló cargos a la IPS Clínica Integral de Emergencias Laura Daniela S.A., por el presunto incumplimiento de los establecido en la resolución 1403 del 2007, Decreto 677 de 1995, Decreto 2200 de 2005, debido a que la IPS habría incumplido lo exigido por la normatividad vigente. Es decir, que la Clínica Laura Daniela compró medicamentos en establecimientos no autorizados.
Antecedentes
Tres de las madres, a quienes les entregaron sus bebés muertos después de ingresar a UCI de la Clínica Laura Daniela, denunciaron los casos ante el programa Séptimo Día de Caracol Televisión.
Dilia Gámez explicó que los pulmones de su hijo no estaban completamente desarrollados, por eso el menor necesitaba un surfactante pulmonar, con el fin de que los órganos comenzaran a desarrollarse. Ese medicamento fue Survanta, que según Gámez, el niño recibió durante 14 días que estuvo en la UCI neonatal: “Durante esos días presentó crisis respiratoria”. Finalmente, el pequeño falleció el 3 de noviembre de 2016, a las 10:30 de la noche.
En lo denunciado por Séptimo Día, se indicó que en Colombia de cada 10 medicamentos, tres o cuatro pueden ser falsificados. Advirtieron también que para la Secretaría de Salud de Cesar los “bebés atendidos en Laura Daniela no fallecieron por esa causa”.
La Policía Fiscal y Aduanera indicó que medicamentos homeopáticos, antiinflamatorios, quemadores de grasa, tratamientos para neonatos, para el cáncer, psiquiátricos, viagra, antigripales y anticonceptivos femeninos, han sido los más falsificados en 2017.
Cabe recordar que en enero de este año, este medio de comunicación registró la noticia de que el CTI de la Fiscalía, con el acompañamiento de un perito en representación de una multinacional farmacéutica, allanó varios centros asistenciales en Valledupar, entre ellos la Clínica Laura Daniela, en donde encontraron un medicamento adulterado especial para niños prematuros.
“Según Miller Cañón perito investigador de laboratorios farmacológico procedente de Bogotá, las muestras realizadas al medicamento se comprobó la falsificación”, declaró por medio de RPT Noticias.
En el marco del procedimiento judicial no se registraron capturas de personal adscrito a la institución prestadora de salud, ni a quienes suministraban el medicamento.
La Secretaría de Salud dijo estar actuando “bajo términos y competencias legales en caso de medicamento presuntamente adulterado”.
Con respecto a lo denunciado por laboratorios Abbviese, mediante el cual se investiga si el medicamento Survanta habría sido adulterado y utilizado para el suministro a pacientes neonatos en la Clínica Integral de Emergencias Laura Daniela de Valledupar, la secretaria de Salud, Carmen Sofía Daza Orozco, informó que desde el momento en que su sectorial tuvo conocimiento de los hechos se iniciaron las acciones de acuerdo a su competencia.
La Secretaría de Salud indicó que realizó visitas de seguimiento en las diferentes instituciones prestadoras de salud que cuentan con el servicio de UCI neonatal habilitado, no encontrando méritos para iniciar investigación alguna diferente a la ya iniciada por el CTI de la Fiscalía.
La Fiscalía General de la Nación oficiará hoy, a partir de las 8:30 de la mañana, una conferencia de prensa para tratar las denuncias sobre presuntos medicamentos falsificados en Valledupar.
La denuncia ante el Invima fue de Abbvie, los mismos que por medio de un delegado elevaron queja en la Secretaría de Salud Departamental, el 15 de noviembre de 2016.
“El 25 de noviembre un niño prematuro, de bajo peso al nacer, necesitaba que se le suministrada Survanta, la neonatóloga que lo aplica se percata que las características físicas y químicas del medicamento son diferentes a las acostumbradas”: Armando Almeira.
Por Carlos Mario Jiménez
[email protected]